Мы — компания «Попсикуб Рус», филиал международной компании Popsicube Fovea, занимаемся развитием продуктовых портфелей фармацевтических компаний. Из всей команды опыт теоретического знакомства с Agile был только у меня в виде двух непродолжительных онлайн-тренингов agile-коучей Nate Dinet и Дмитрия Маева. Тренинги были очень информативными, но за два часа непросто приобрести глубокое понимание, как методологию увязать с практикой.
Таким образом, к началу работы в проектах пополнения продуктового портфеля, представление об Agile у меня оставалось сугубо теоретическим: «Agile нужен для сложных, запутанных проектов. В рамках Agile организовывается фокус-группа, которая работает над проектом так, как будто проект уже достиг более поздней стадии. Задача фокус-группы — создать в усеченном виде рабочую модель продукта».
Зачем создавать на ранней стадии проекта усеченную рабочую модель продукта, который будет на поздней стадии, — было не очень понятно. Что такое «сложные, запутанные» проекты — тоже было неясно.
Как все начиналось
Осенью 2019 наша команда приступила к оценке новых продуктов для вывода на российский рынок. За основу мы взяли модель классического проектного подхода, по которой этот процесс традиционно выстраивается в фармацевтических компаниях.
В рамках этой модели первым звеном является менеджер отдела развития бизнеса или менеджер продуктового портфеля — специалист с двумя видами компетенций. Во-первых, это компетенции в «матчасти», позволяющие разбираться в научной и практической ценности лекарственных средств. Во-вторых, компетенции по анализу рынка, построению прогноза продаж, построению отчета о прибылях и убытках, составлению бизнес-планов.
Идеальный кандидат — человек с двумя высшими образованиями: медицинским или фармацевтическим и экономическим, имеющий опыт работы в оценке коммерческого потенциала лекарственных средств.
Для помощи менеджеру продуктового портфеля в фармкомпаниях организовано кросс-функциональное взаимодействие: менеджер может обращаться за консультациями в медицинский отдел, отделы регистрации, маркетинга, продаж. После того, как менеджер портфеля, посоветовавшись при необходимости с коллегами из указанных отделов, составляет мнение о коммерческом потенциале продукта, продукт переходит на следующие этапы, включающие заключение договора о приобретении лицензии, глубокую проработку маркетинговой стратегии, стратегии регистрации, тщательную подготовку медицинской информации, взаимодействие с лидерами мнений, лонч…
Что пошло не так
Мы обнаружили, что результативность нашей работы не одинакова для двух разных групп продуктов.
Первая группа — это дженерики и биосимиляры (копии) популярных препаратов, которые уже продаются в России. Допустим, мы собрались выводить на российский рынок препарат железа для лечения анемии. На сайте Государственного реестра лекарственных средств можно видеть, что в России зарегистрировано 42 препарата железа 22 фармацевтических компаний. В платных базах данных, созданных аналитическими компаниями (база IMS компании IQVIA, база DSM компании DSM Group), можно найти объем продаж в упаковках и рублях по каждому из 42 препаратов в 2019, 2018, 2017 годах и ранее. На основе этой информации обученный специалист легко делает прогноз: какую долю рынка у 22 компаний-конкурентов мы сможем забрать, какими будут продажи нашего продукта, который станет 43 препаратом железа на российском рынке.
Для первичной оценки коммерческого потенциала продуктов этой группы требуется только наличие доступа к базе данных (IMS или DSM) и одного обученного специалиста, который умеет делать прогноз продаж. И действительно, наш менеджер продуктового портфеля быстро и уверенно справлялся с оценкой потенциала дженериков и биосимиляров.
Совсем по-другому дело обстояло со второй группой продуктов, которая включала препараты более сложные для первичной оценки:
1. Старые оригинальные (инновационные, референтные) препараты, которые уже продаются в других странах, но еще отсутствуют на российском рынке. В эту же группу попадают дженерики в ситуации, когда на российском рынке нет ни оригинального, ни дженериковых препаратов с данным действующим веществом.
«Старые» — означает, что продукту 10, 15, 20, 40 лет, на мировом и российском рынке продаются более новые лекарственные средства. В то же время, новые средства не являются заменой старым, и не сразу ясно, где место старого препарата в схемах лечения, и какую долю рынка он может занять.
2. Препараты, которые ранее были зарегистрированы и продавались в России, имели маленький объем продаж, ушли с рынка по каким-либо причинам, а теперь компания-правообладатель хочет снова выходить на российский рынок.
3. Препараты, у которых на российском рынке есть плохо продающиеся конкуренты или аналоги. Либо конкуренты плохо продавались и ушли с российского рынка.
4. Лекарственные средства для таких заболеваний, для которых в официальной медицине не разработано четких клинических рекомендаций и стандартов лечения и профилактики, или существующие стандарты неполные, содержат скудную информацию.
5. Препараты/медицинские изделия с нестандартным инновационным механизмом действия, который не позволяет сразу понять, будет ли данный продукт дополнением к уже существующим на рынке способам лечения, или он будет являться их конкурентом.
При оценке продуктов этой группы ситуация развивалась по одному из следующих сценариев:
1. Менеджер портфеля не привлекал коллег из других направлений.
Он делал первичное заключение о коммерческом потенциале самостоятельно. Однако, в отличие от «простых» дженериков, в случае со «сложными» препаратами такое заключение часто было ошибочным, так как без глубокой проработки многие факторы не учитывались, либо учитывались неверно. Например, в конкуренты записывались препараты, которые конкурентами не являются, не оценивались причины маленьких объемов продаж конкурентов или неправильно определялась целевая группа пациентов для препарата.
Характерно, что все ошибки совершались в сторону занижения потенциала продукта — когда менеджер портфеля отсеивал хороший препарат как неперспективный.
2. Менеджер портфеля делал запросы коллегам из других направлений.
Например, медицинскому советнику. Медицинский советник, ознакомившись с продуктом, сообщал, что ему требуется проанализировать около сотни публикаций по препарату и конкурентам, а это займет 30 часов времени.
Так как медицинский советник в рамках своей зарплаты выполняет работу по научной поддержке различных проектов организации, то приступить к детальной оценке литературы по новому продукту он мог только через месяц, а завершить — через два месяца. Таким образом, в течение этих двух месяцев менеджер продуктового портфеля не мог сформировать мнение о коммерческом потенциале продукта, и проект «простаивал».
3. Идеальная ситуация: менеджер в одиночку верно оценивал потенциал продукта.
Либо у медицинского советника и других специалистов находилось достаточно времени на экспертизу препарата. В этом случае мы быстро получали правильное заключение о коммерческом потенциале продукта.
Проще говоря, при работе в классическом проектном подходе в случае «сложных» продуктов мы с одинаковой частотой получали результат:
- быстро и правильный;
- быстро, но неправильный;
- правильный, но медленно.
Мы поставили цель — быстро получать максимально правильный результат. Нам важно получать результат быстро, так как препарат могут «перехватить» компании-конкуренты, заключив с правообладателем продукта лицензионный договор. И важно получать результат максимально точный: иначе, записывая хорошие продукты в неперспективные и отказываясь от них, мы лишаем себя прибыли.
Что мы предприняли
Стало очевидным, что для оценки коммерческого потенциала продуктов «сложной» группы с самого начала необходимы одновременные действия:
- Вдумчивая работа медицинского советника, который десятки часов анализирует научную литературу по препарату, по способам лечения заболевания, для которого показан препарат, по возможным конкурентам. Цель — получить максимально точное представление об объективной медицинской ценности продукта и его преимуществах/недостатках по сравнению с конкурентами.
- Тесное взаимодействие команды с врачами и медицинскими учреждениями. Цель — получить обратную связь по всему, что связано с медицинским применением продукта; также — получить понимание количества пациентов, востребованности продукта. Для инновационных продуктов — работа с научным медицинским сообществом на предмет включения препарата или медицинского изделия в стандарты лечения или профилактики.
- Работа маркетолога по разработке стратегии продвижения продукта и анализу стратегии конкурентов, анализу причин плохих продаж конкурентов. Цель — получить понимание, по каким показаниям, среди какой ЦА продвигать продукт.
- Работа менеджера по доступу препаратов на рынок: проведение фармакоэкономического анализа, определение списка программ бюджетного финансирования, в которые можно включить продукт, оценка возможностей и препятствий в государственных закупках.
Таким образом, для «сложных» продуктов мы стали с самого начала формировать фокус-группу, включающую менеджера продуктового портфеля, специалиста по доступу препаратов на рынок, медицинского советника и маркетолога. Эта фокус-группа совместно прорабатывает продукт так, как будто он уже на более поздней стадии. Мы делаем допущение, будто уже приняли продукт в портфель, и теперь выводим его на рынок.
Будет правильным сказать, что мы на этапе оценки коммерческого потенциала продукта сразу проделываем подготовку к лончу и своеобразный мини-лонч.
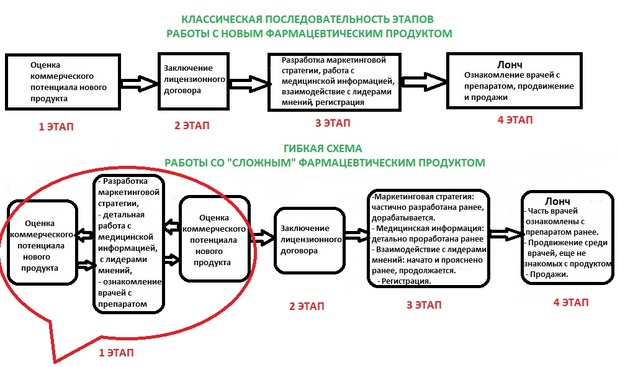
Работа фокус-группы продолжается 2-3 недели. Важное условие работы фокус-группы — участники должны посвящать проработке проекта столько времени, сколько необходимо, отставив в сторону другие дела.
В конце этого этапа формируется реальная модель продукта в том виде, в каком он будет выводиться на рынок после получения регистрационного удостоверения.
Что стало
Создание фокус-группы позволило нам ускорить оценку коммерческого потенциала «сложных» продуктов в два раза и снизить риск ошибок, когда перспективность продукта остается незамеченной.
Здесь следует коснуться такого аспекта, как затраты. Создание фокус-группы повышает стоимость процедуры оценки коммерческого потенциала продукта.
У фармацевтических компаний, работающих на территории России, чаще всего офис находится в Москве, реже — в Санкт-Петербурге. Соответственно, на позиции медицинских советников, маркетологов, менеджеров по продукту, менеджеров продуктового портфеля фармкомпании нанимают жителей Москвы, которые ездят на работу в офис 5/2.
По отчету Hays за 2018 год, средняя зарплата медицинского советника (Medical Advisor) в Москве составляет 160 тысяч рублей, менеджера по развитию бизнеса (менеджера по развитию продуктового портфеля) — 350 тысяч рублей, менеджера по продукту — 150 тысяч рублей для начинающего, 210-230 тысяч для опытного.
Типичная фармацевтическая компания с московским офисом и office based сотрудниками способна применять гибкий подход к оценке новых продуктов, если у работников не очень высокий уровень повседневной нагрузки. В этом случае члены команды смогут быстро найти достаточное количество времени на новый проект в рамках стандартной зарплаты.
Если же в фармкомпании большие нагрузки, то сотрудники не смогут быстро находить десятки часов для глубокой проработки нового проекта в рамках фокус-группы. Компании придется или отдельно доплачивать работникам за сверхурочную работу, или привлекать дополнительные ресурсы: фрилансеров, индивидуальных предпринимателей, нанимать людей в штат. В любом случае, процесс будет сопровождаться повышением затрат.
Нам удалось снизить стоимость оценки новых продуктов за счет внедрения удаленных команд: у нас в режиме домашнего офиса работают сотрудники, проживающие в регионах.
Привлечение региональных специалистов вместо московских позволяет снижать затраты на ФОТ в два раза. При этом лояльность удаленного работника выше: у жителей регионов нет большого выбора фармкомпаний-работодателей, не считая вакансий медпредставителя — «полевого» торгового представителя по лекарствам. Поэтому для человека ценно получить возможность работать по той специальности, по которой ему хочется — продактом, медицинским советником, менеджером портфеля.
Следует отметить, что создание фокус-групп, отлично подходящее для «сложных» продуктов, финансово не оправдано для «простых» продуктов — как в примере с препаратами железа.
Текст участвует в конкурсе «Историй успеха»












Елена, спасибо за статью,
не вполне понятен следущий момент: если клинические исследования включены в 3 этап (регистрация), то почему им предшествует заключение лицензионного договора, ведь по существу продукта еще нет?
Александр, а это зависит от того, как компания-правообладатель и компания-партнер договорятся.
Бывает, что российская компания сразу платит лицензионный взнос, когда продукт не зарегистрирован. Соответственно, если Минздрав по каким-либо причинам отказывает в регистрации продукта, то российская компания теряет деньги, и в этом ее риск.
Бывает, что зарубежная компания сама занимается регистрацией продукта в России, а потом продает лицензию - но в этом случае стоимость лицензии выше.
И еще разные модели бывают.